 A Biofizikai és Sejtbiológiai Intézetben kutató Nagy Lőrinc, Mezősi-Csaplár Marianna, Rebenku István, Vereb György és Szöőr Árpád eredményei segítenek pontosabban leírni az új típusú, génmódosított immunsejteken alapuló célzott daganatterápiák mechanizmusait. A kiméra antigén receptor (CAR) T sejtek hatékonysága a daganatterápiában korlátozott, mert sok esetben a daganatsejtek terápiarezisztenssé válnak a célmolekula expressziójának megszűnte miatt. Az univerzális CAR (UniCAR) T sejtek megoldást kínálnak erre a problémára olyan módon, hogy adapter molekulákon, például biotinált antitesteken keresztül ismerik fel a molekuláris célpontjukat, lehetővé téve párhuzamosan több célpont támadását is egyetlen CAR T sejt készítmény által.
A Biofizikai és Sejtbiológiai Intézetben kutató Nagy Lőrinc, Mezősi-Csaplár Marianna, Rebenku István, Vereb György és Szöőr Árpád eredményei segítenek pontosabban leírni az új típusú, génmódosított immunsejteken alapuló célzott daganatterápiák mechanizmusait. A kiméra antigén receptor (CAR) T sejtek hatékonysága a daganatterápiában korlátozott, mert sok esetben a daganatsejtek terápiarezisztenssé válnak a célmolekula expressziójának megszűnte miatt. Az univerzális CAR (UniCAR) T sejtek megoldást kínálnak erre a problémára olyan módon, hogy adapter molekulákon, például biotinált antitesteken keresztül ismerik fel a molekuláris célpontjukat, lehetővé téve párhuzamosan több célpont támadását is egyetlen CAR T sejt készítmény által.
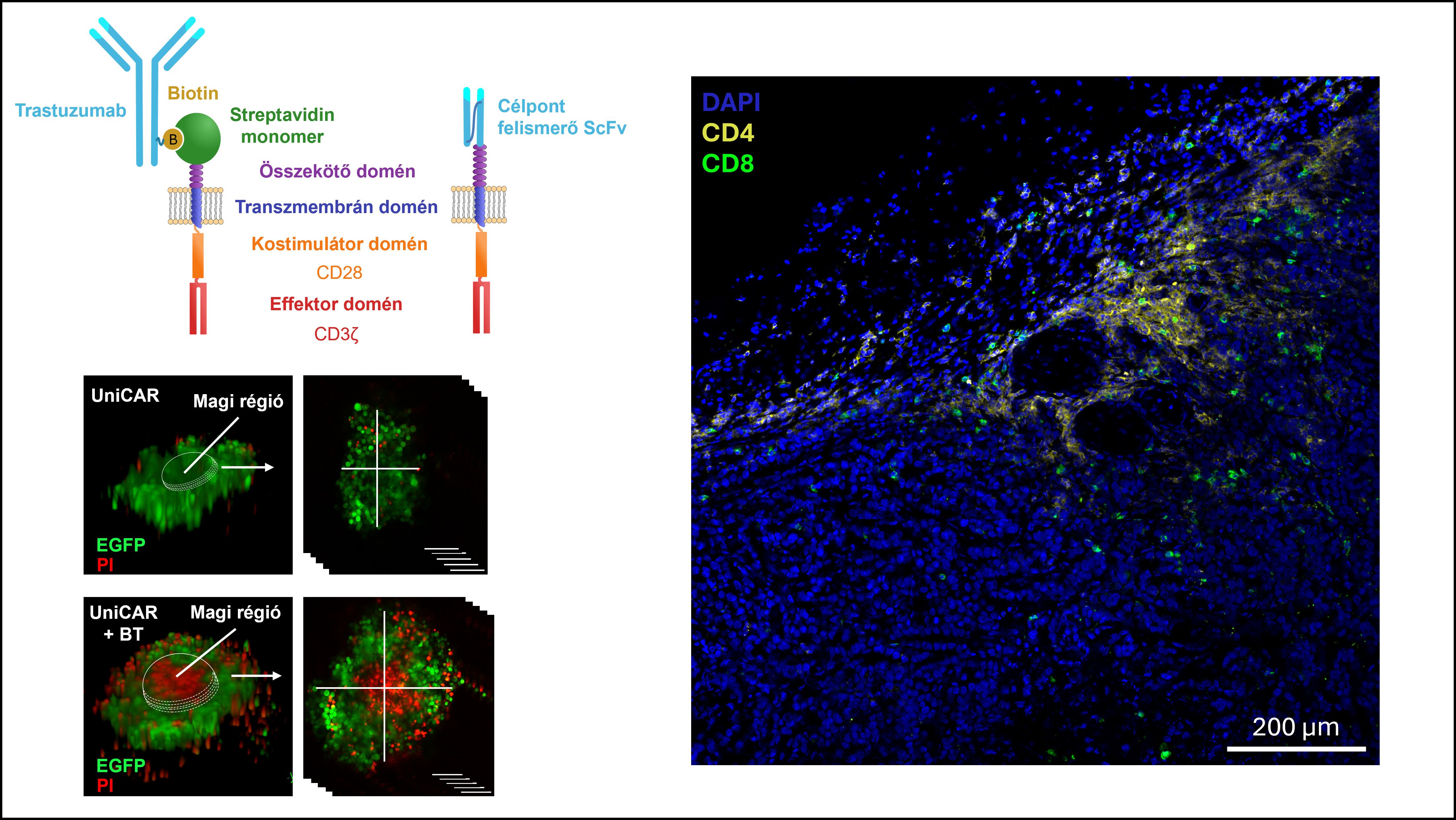
A kutatócsoport korábban bizonyította, hogy a konvencionális CAR T sejtek képesek áthatolni a tumorok jól fejlett extracelluláris mátrixán (ECM), amely gátolja a terápiás antitestek bejutását, így biztosítva védettséget a tumornak. Jelen kutatásukban azt vizsgálták, hogy a szintén antitestek által irányított UniCAR T sejtek is képesek-e a konvencionális CAR T sejtekéhez hasonló tumorpenetrációra. A létrehozott UniCAR konstrukcióban egy biotinkötő streptavidin 2 monomer (mSA2) biztosította a biotinált trastuzumab (BT) antitesthez való kapcsolódást és azon keresztül a HER2 célpont (közvetett) felismerését.
A BT-vel célra irányított UniCAR T sejtek hatékony és specifikus immunreakciót mutattak mind a sejttenyésztő edény felszínéhez kötött, mind a sejtmembránban kifejeződő HER2 célpont jelenlétében, és behatoltak a tumor szferoidok központi régiójába is, elpusztítva a daganatsejteket. Az in vivo kísérletek bizonyították, hogy az UniCAR T sejtek fiziológiás körülmények között képesek azonnal megkötni a keringő BT antitesteket és ezt követően célba venni a HER2+ tumor xenograftokat. Ugyanakkor a natív HER2 és biotin jelenléte miatt a tüdőben ez a konstrukció mellékhatásokat mutatott.
Az eredmények alapján a biotinhoz hasonló, de a szervezetben nem kifejeződő adaptermolekulák alkalmazása jelenthet optimális megoldást az antitest terápiára rezisztens, magas antigén heterogenitást mutató tumorok ellen. Ugyanakkor kiemelt fontosságú, hogy az UniCAR nagy affinitással kösse az adatper molekulát, ezzel biztosítva a tumor penetrációt, amire az adapter molekula önmagában nem volna képes.